Причины отсутствия имплантации в ЭКО и ЕЦ - интересная статья
Библиотека: статьи, полезная информация. Стихи, видео и фильмы про ЭКО.Собираюсь на свое первое ЭКО и перед этим проверяю все, что можно проверить) Про мутации гемостаза и антитела наслышана, нахожусь в процессе сдачи. Наткнулась на любопытный материал, букв много, поэтому сократила 
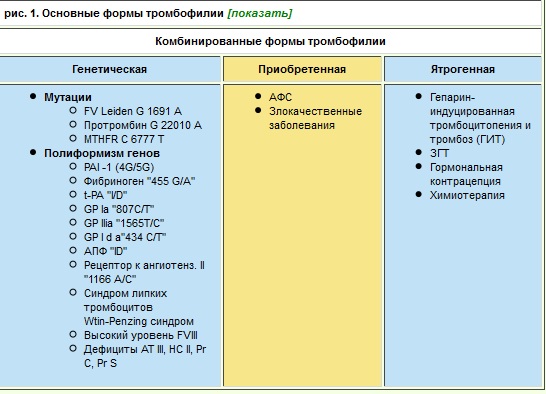
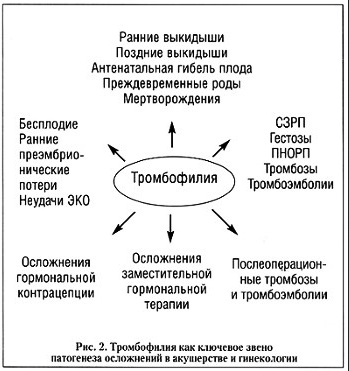
В мировой литературе последних лет все чаще репродуктивные потери объединяются в так называемый "синдром потери плода", включающий:
- один или более самопроизвольных выкидышей на сроке 10 недель и более (включая неразвивающуюся беременность);
- мертворождение;
- неонатальная смерть, как осложнение преждевременных родов, тяжелого гестоза или плацентарной недостаточности;
- три или более самопроизвольных выкидыша на преэмбрионической или ранней эмбрионической стадии, когда исключены анатомические, генетические и гормональные причины невынашивания.
 Если ранее привычное невынашивание беременности (привычный выкидыш, рецидивирующий спонтанный аборт) определялось как 3 и более беременностей, заканчивающихся самопроизвольным выкидышем, то в последние годы для постановки диагноза привычного невынашивания считают достаточным 2 повторных эпизода самопроизвольного прерывания беременности на ранних сроках.
Если ранее привычное невынашивание беременности (привычный выкидыш, рецидивирующий спонтанный аборт) определялось как 3 и более беременностей, заканчивающихся самопроизвольным выкидышем, то в последние годы для постановки диагноза привычного невынашивания считают достаточным 2 повторных эпизода самопроизвольного прерывания беременности на ранних сроках. На сегодняшний день под антифосфолипидным синдромом (АФС) понимают симптомокомплекс, сочетающий определенные клинические признаки и лабораторные данные: наличие антифосфолипидных антител в сочетании с артериальными и венозными тромбозами, синдромом потери плода, иммунной тромбоцитопенией и/или неврологическими расстройствами.
На сегодняшний день под антифосфолипидным синдромом (АФС) понимают симптомокомплекс, сочетающий определенные клинические признаки и лабораторные данные: наличие антифосфолипидных антител в сочетании с артериальными и венозными тромбозами, синдромом потери плода, иммунной тромбоцитопенией и/или неврологическими расстройствами. - В последние годы стали рассматриваться и изучаться нетромботические эффекты тромбофилии в патогенезе акушерских осложнений еще на этапе имплантации плодного яйца и в раннюю эмбрионическую фазу. Имплантация, инвазия трофобласта и дальнейшее функционирование плаценты представляются многоступенчатыми процессами эндотелиально-гемостазиологических взаимодействий со сложной аутокринно-паракринной регуляцией, которые объективно нарушаются при тромботической тенденции и в случае генетических дефектов свертывания. Хотелось бы заметить, что беременность является состоянием, которое можно назвать своеобразным "экзаменом" на наличие скрытой приобретенной (АФС) или генетической тромбофилии, поскольку она сама сопровождается физиологической гиперкоагуляцией и способствует реализации скрытой тромбофилии не только в форме тромбозов и тромбофилий, но и типично акушерских осложнений.
Согласно нашему исследованию, роль тромбофилии (в том числе различных ее форм) неодинакова в патогенезе и структуре репродуктивных потерь в рамках синдрома потери плода. Так, циркуляция АФА чаще обнаруживалась у пациенток с ранними выкидышами (43,1%), соответственно у 22,4% пациенток с поздними выкидышами и у 35,7% - с ранними преэмбрионическими потерями. В то же время мутации FV Leiden чаще имела место у пациенток с поздними выкидышами (15%). Мутация протромбина G20210A встречалась достоверно реже во всех группах репродуктивных потерь (по сравнению с АФА, FV Leiden п MTHFR С677Т) и составила 4,2% и 3,0% в группах ранних и поздних выкидышей соответственно. Наиболее распространенной у пациенток с синдромом потери плода оказалась мутация MTHFR С677Т, которая соответственно составила 41,2% у пациенток с синдромом потери плода. Одним из наиболее важных результатов исследования нам представляется обнаруженная высокая частота мультигенных форм тромбофилии (два и более дефекта) у обследованных пациенток с синдромом потери плода. Суммарно мультигенная тромбофилия у всех пациенток с синдромом потери плода составила 55,7%: в группе ранних выкидышей - 55,6%, в группе поздних выкидышей -62,3%, в группе ранних преэмбриональных потерь - 39,3%. При этом характерной особенностью мультигенных форм тромбофилии явилась высокая частота полиморфизма различных генов тромбофилической направленности.
При анализе клинических проявлений тромбофилии у пациенток с синдромом потери плода также была выявлена следующая особенность: тромбозы в анамнезе имели пациентки либо с гомозиготной мутацией FV Leiden, либо с сочетанием АФА и FV Leiden, мутацией протромбина С20210А или полиморфизмом PAI-1 4G/4G. Кроме того, тромбозы отмечались и у пациенток с более чем 3 гомозиготными формами полиморфизма генов (PAI-1, гена фибриногена и/или тромбоцитарных рецепторов). С нашей точки зрения, наиболее яркой моделью для изучения нетромботических эффектов тромбофилии являются ранние преэмбрионические потери. Крайне интересные результаты были получены нами именно в группе пациенток с преэмбрионическими потерями. Характерно, что большинство женщин этой группы лечились изначально от бесплодия. При этом у большинства из них уже были неоднократные неудачные попытки экстракорпорального оплодотворения (ЭКО).
Анализ тромбофилии показал, что у 60,7% пациенток имела место тромбофилия. При этом наиболее часто обнаруживался полиморфизм PAI-1 (50,0%), в том числе в сочетании с дисфибриногенемией и/или полиморфизмом АПФ "I/D", а также мутация MTHFR С677Т (35,7%), АФА (35,7%) и мультигенные формы тромбофилии (39,3%). Характерно, что у женщин с гомозиготным полиморфизмом PAI-1 4G/4G, синдромом поликистозных яичников и/или метаболическим синдромом имело место значительное повышение уровня PAI-1. Это важное наблюдение позволяет предположить, что, возможно, в патогенезе бесплодия (а точнее, часто нераспознанных преэмбрионических потерь) при СПКЯ и метаболическом синдроме, помимо эндокринных причин, крайне важную роль играет наличие одновременно высокого уровня PAI-1.
-
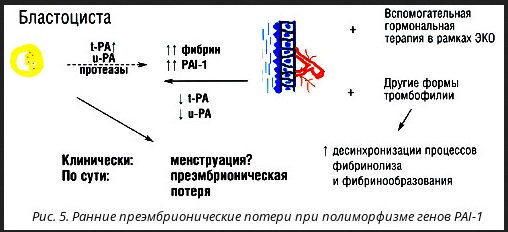
Ранние преэмбрионические потери в основном связаны с дефектами имплантации плодного яйца. Процесс имплантации начинается на 6-й день после овуляции и представляет собой не односторонний процесс активной инвазии, а своеобразный энзиматический "обмен" между бластоцистой и эндометрием, для которого необходима гормональная стимуляция и определенная "зрелость" эндометрия. В процессе подготовки к имплантации под влиянием прогестерона в эндометрии происходит повышение содержания ингибитора активации плазминогена типа 1 (PAI-1), тканевого фактора (TF) и снижение уровня активаторов плазминогена тканевого и урокиназного типов, металлопротеаз матрикса и вазоконстриктора - эндотелина 1. Эти физиологические механизмы регуляции гемостаза, фибринолиза, экстрацеллюлярного матрикса и сосудистого тонуса направлены на предотвращение образования геморрагии при дальнейшей инвазии трофобласта. Со своей стороны, бластоциста синтезирует активаторы плазминогена тканевого и урокиназного типа и протеазы, которые необходимы для разрушения экстрацеллюлярного матрикса в процессе имплантации. Их излишний синтез, в свою очередь, регулируется хорионическим гонадотропином (ХГ). В процессе "дозированного" разрушения матрикса под действием ферментов, выделяемых бластоцистой, клетки эндометрия, которые содержат определенное количество экстраваскулярного фибрина, не фагоцитируются, а как бы "отодвигаются" посредством "контактного ингибирования". Эта фаза процесса имплантации носит название "аваскулярной" или иначе - "гистиотрофной". Следует отметить, что это наиболее уязвимая фаза имплантации: часто такие факторы, как вирусы, токсины, антитела и пр., могут непосредственно влиять на полноценность имплантации. С точки зрения влияния тромбофилии наиболее ярким примером являются полиморфизм PAI-1 и другие генетически обусловленные дефекты фибринолиза и АФС

Если же рассматривать этот вопрос в контексте перечня неудач ЭКО, то, с нашей точки зрения, помимо неучета тромбофилии, дополнительно негативную роль играет вспомогательная терапия с массивной гормонотерапией. В ряде случаев у пациенток с диагнозом бесплодия могут иметь место ранние преэмбрионические потери, которые клинически маскируются нерегулярным менструальным циклом.
Возвращаясь к эффектам тромбофилии, следует отметить, что страдают не только ранняя (аваскулярная) фаза имплантация, но и более поздние этапы имплантации (гемотрофная фаза) и плацентации. Гемотрофная (васкулярная) фаза имплантации начинаются с 12 дней после овуляции: между пролиферирующими клетками трофобласта начинают образовываться лакуны, которые в дальнейшем будут увеличиваться, сливаться и преобразовываться в межворсинчатое пространство плаценты. Именно в эту фазу начинается активный контакт с плазмой матери: трофобласт внедряется (разрушая их) в тонкостенные материнские сосуды, из которых кровь свободно изливается в лакуны трофобласта. К 21 дню после овуляции ворсины трофобласта уже достаточно васкуляризированы и можно констатировать факт установления маточно-плацентарного кровотока. Факторы, обеспечивающие инвазию трофобласта и нормальное развитие плаценты на ранних стадиях очень многообразны: факторы роста, цитокины, интегрины, молекулы адгезии, антигены комплекса гистосовместимости (преимущественно класса 1) и др. Тромбофилия (в том числе вызванная АФА) напрямую или опосредованно влияет на процесс имплантации и ранние эмбрионические стадии.
Отдельно хотелось бы обсудить роль антифосфолипидных антител в патогенезе синдрома потери плода, поскольку эффекты АФА чрезвычайно многообразны в отличие от изолированной формы генетической томбофилии, что обусловлено, по-видимому, большей гетерогенностью различных антител, объединенных общим термином "антифосфолипидные антитела". Именно поэтому наиболее неблагоприятен прогноз при сочетании АФС с генетической тромбофилией: в таких случаях протромботическая тенденция становится непропорционально выше и реализация возможна не только в форме тромботического поражения микроциркуляции и синдрома потери плода, но и в форме макротромбозов. Тромбирование сосудов микроциркуляторного русла в условиях тромбофилии ответственно за широкий спектр акушерских осложнений - от ЗВРП до АГП, мертворождений и ПОНРП. В то же время неблагоприятный фон имеет место уже с момента имплантации и дифференцировки трофобласта.
Повреждающее действие АФА может осуществляться несколькими путями:
- изменяются адгезивные характеристики предимплантационого эмбриона;
- нарушается слияние синцития;
- снижается глубина инвазии трофобласта;
- подавляется продукция хорионического гонадотропина;
- усиливаются тромботические тенденции за счет предоставления матриц для реакций свертывания.
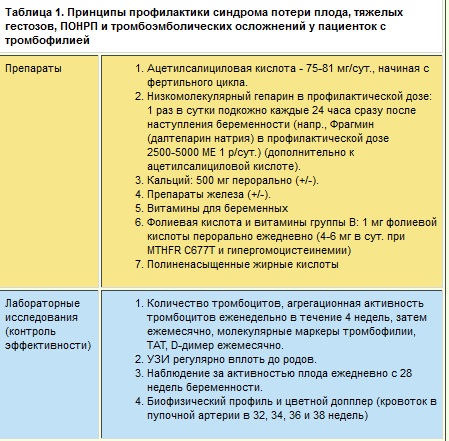
В связи с ключевой ролью тромбофилии в патогенезе синдрома потери плода, гестозов, ПОНРП и, конечно, тромбоэмболизма, профилактика этих осложнений подразумевает применение противотромботических препаратов. Тем не менее, учитывая, что нарушения, связанные с тромбофилией и неадекватным образованием фибрина, начинают формироваться еще на этапе имплантации оплодотворенной яйцеклетки, инвазии трофобласта, формирования плаценты, важно еще до зачатия проводить профилактику возможных более поздних осложнений.
Наш опыт свидетельствует, что патогенетически обоснованная профилактика позволяет во всех случаях предупредить рецидив тромбоза и в абсолютном большинстве случаев (92-96%) значительно улучшить исходы беременности. При этом достоверно лучшие исходы имеют место у пациенток, которые получают противотромботическую профилактику с ранних сроков беременности и в фертильном цикле. А.Д. Макацария, В.О. БицадзеММА имени И.М. Сеченова Источник здесь