Химические опыты. Часть 2
УчебноеА сегодня мы поговорим непосредственно про химические опыты в домашних условиях.

Но для начала определимся с тем, что такое химическая реакция и почему она происходит.

Мы уже говорили, что нас окружают вещества, которые в свою очередь состоят из молекул, а молекулы - из атомов.
Для того, чтобы атомы соединились между собой, они должны измениться - отдать или забрать электроны.
Электроны - одна из составляющих атома. Они вращаются вокруг атомного ядра. На картинке ниже большой шарик в центре - атомное ядро, а маленькие шарики вокруг него - электроны.

Структура атома напоминает строение нашей Солнечной системы.
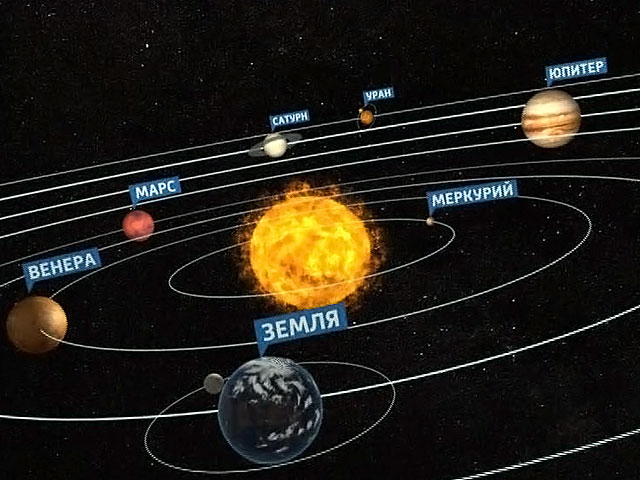
Максимальное количество электронов на внешней орбите - 8. Минимальное - 1.
Наш мир стремиться к стабильности. Поэтому и атомы стремятся достичь равновесия - собрать на своей внешней орбите 8 электронов или отдать "лишние" электроны.
Атомы, которые отдают электроны, называются восстановители. К таким атомам в основном относят металлы - литий, натрий, калий, кальций и т.п.
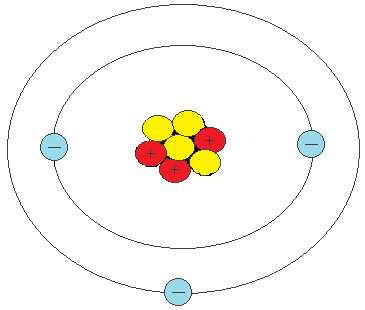
Атомы, которые забирают электроны у других, называются окислители. К ни относят неметаллы - хлор, бром, кислород, фтор и т.п.

Посчитайте шарики-электроны на внешнем круге: у восстановителей на самом далекой от центра орбите электронов больше, у восстановителей - меньше.
Кроме того, в природе есть атомы, которые в одних условиях ведут себя как окислители, а в других как восстановители. Самый известный из таких элементов - алюминий

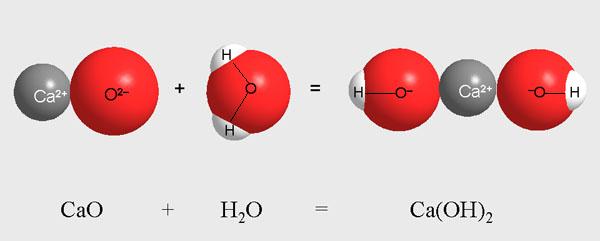
Самое известное амфотерное (именно так химики называют элементы и вещества с двойственной природой) - вода

Именно взаимодействием окислителей и восстановителей и объясняется возможность химической реакции, которые по сути являются превращением одних веществ в другие.
Одним из первых классификацию химических элементов в зависимости от их свойств предложил русский химик Дмитрий Иванович Менделеев
Он обнаружил, что некоторые элементы ведут себя одинаково, а их свойства зависят от атомного веса. На основании своих наблюдений он составил периодическую систему химических элементов, которой мы пользуемся по сей день.

От теории перейдем к практике.
1. Фиолетовый крахмал.
Самый простой опыт и безопасный опыт, который можно проводить дома, это эксперимент с крахмалом и йодом.
Ход опыта.
В воду добавляем крахмал и взбалтываем. Получается мутная сероватая жидкость, т.к. крахмал не растворяется в воде.
Теперь добавим в нашу взвесь капельку йода.
Жидкость станет фиолетовой.
Почему так происходит?
Крахмал - сложное соединение, состоящее из нескольких хвостиков. Один из этих хвостиков реагирует с йодом и меняет окраску всей взвеси.

2. Варим гель.
И снова делаем взвесь крахмала с водой. Но теперь мы будем его нагревать,постоянно помешивая. При постепенном нагревании "жидкий" крахмал станет вязким, похожим на гель или клей.
Что произошло? Мы помним, что крахмал - сложное вещество, состоящие из нескольких хвостиков. Один из таких хвостиков способен впитывать воду и набухать. Одна молекула способна впитать в 2-4 раза воды больше, чем она сама. Вот это впитывание воды и набухание крахмального зерна мы и наблюдаем.

Нагретый таким образом крахмальный раствор можно использовать вместо клея. Но, если "гель" перегреть, то клейкость крахмала резко упадет.
3. Пузырьки.
Чтобы выпечка была пышной, мы добавляем в нее пекарский порошок. А пекарский порошок - это сухая смесь соды и лимонной кислоты, которые при попадании на них жидкости начинают реагировать. Посмотрим, что будет, если мы перенесем эту реакцию из пирожков и печенек в банку.
Итак, возьмите по столовой ложке соды и лимонной кислоты. Смешайте их в прозрачной банке. Добавьте пару ложек воды и посмотрите, что произойдет.
А произойдет следующее: на поверхности нашей смеси начнут активно образовываться пузырики. Одновременно, если прислушаться, будет слышно шипение.

Почему так происходит?
Сода состоит из метала натрия и остатка угольной кислоты. Когда мы добавляем к ней лимонную кислоту, то остаток угольной кислоты заменяется на остаток лимонной. Получается натриевая соль лимонной кислоты, которая называется цитрат натрия. Остаток угольной кислоты пытается восстановиться до угольной кислоты. Но угольная кислота крайне не стабильна и распадается на углекислый газ и воду. Именно с выделением углекислого газа и связаны пузырьки на поверхности смеси. "Шипит" смесь тоже из-за выделения углекислого газа.
А теперь пара веселых подопытов с нашими приятелями - содой и лимонной кислотой.
Сначала нам необходимо подготовить соду.
Обычно сода - это порошок. Мы будем делать из нее камешки.
Для содовых камешков нам нужно насыпать соду в любую плошку и аккуратно смочить ее водой из пульверизатора. Смачивать будем аккуратно, чтобы наша сода намокла, но не начала растворяться. Оставим ее высыхать. Когда вода испариться, сода из порошка превратиться в небольшие камешки. И именно эти камешки и комочки мы будем использовать для пары следующих опытов.
Эксперимент 1. Лава-лампа.
Для него нам потребуются вода, пищевой краситель, растительное масло, лимонная кислота, содовые камешки.
Мы помним, что разные жидкости могут смешиваться между собой, образуя растворы. Такие растворы мы видим, например, когда разбавляем чайную заварку водой.
Другие жидкости не смешиваются между собой, а образуют слои. Так происходит с маслом

Масло "плавает" на поверхности воды. И даже если мы хорошенько перемешаем наши жидкости, рано или поздно масло снова будет плавать на поверхности воды.
Для нашего опыта мы сначала подкислим и подкрасим воду: добавим в нее лимонную кислоту и пищевой краситель.
Затем нальем в нашу воду масло и дождемся, пока все масло не поднимется на поверхность воды.
А теперь аккуратно бросаем камешек соды.
У нас начнут образовываться пузырьки, которые будут поднимать нашу подкрашенную воду в масло.

Эксперимент второй. Пена.
Молекулы мыла и шампуня тоже сложны. Они похожи на головастика: головка молекулы не любит воду и отталкивается от нее, а хвостик молекулы воду любит и стремиться к ней. Благодаря этому свойству молекулы мы и можем надувать мыльные пузыри или купаться в ванне с пеной.

И наш следующий опыт будет связан со свойством мыла образовывать пузырики, а углекислого газа помогать мылу это делать.
Итак, в бутылку с широким горлом налить подкисленную воду, добавить ложку жидкого мыла, шампуня и т.п. и бросить туда содовый камешек.
Чтобы опыт удался, заполняйте бутылку максимум на 2/3, лучше на 1/3.
Из бутылки медленно начнет "выпозать" пенная змея.
3. Металл "пьет" йод.
Для этого опыта нам понадобиться любой старый металлический предмет: старые ключи, монеты и т.п. Главное, чтобы они были не блестящими, а покрытыми темно-серым налетом.
Теперь возьмем спиртовой раствор йода и аккуратно капнем его на нашу металлический предмет.
Оставим на некоторое время. Посмотрите внимательно: на металле не остается бурых йодных пятен. Он как будто бы испарился. Кроме того, место, куда мы наливали йод, может стать светлым или наоборот темным. В зависимости от металла.

