Химическое
УчебноеА сегодня мы немного отойдем от биологии и поговорим о химии и физике


Химия - это наука о веществах и их превращениях

А физика - наука о материи, ее свойствах и движении

Физика и химия, как и биология, помогают нам понять окружающий нас мир. Только каждая из них рассматривает свою область знаний.
Все, что нас окружает, состоит из крошечных, невидимых невооруженным глазом, частичек
Атомов

Но и сами атомы не являются единым целым, а состоят из протонов, нейтронов и электронов

Протоны и нейтроны составляют атомное ядро.
Химическая реакция - это отношения между разными атомами, когда атомное ядро не изменяется
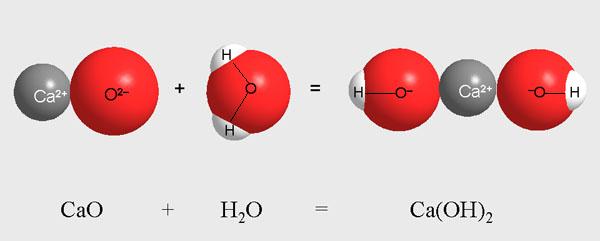
Физическая или ядерная реакция - это изменение самого атомного ядра

В результате ядерных реакций получаются новые атомы.
А в результате химических реакций образуются новые вещества.
Вещество - это несколько атомов, соединенных между собой.
Оно может быть простым, когда атомы в составе вещества одинаковые

К простым веществам относятся кислород, которым мы дышим, графит, из которого состоит грифель простого карандаша, многие металлы

И сложные вещества, когда атомы в составе вещества разные
Вода - это сложное вещество, она состоит из одного атома кислорода и двух атомов водорода.
Соль, которую мы добавляем в пищу, - тоже сложное вещество, которое состоит из одного атома хлора и одного атома натрия.

Большинство веществ, окружающих нас, являются сложными веществами.
Состояния вещества
Практически любое вещество может находиться в трех основных состояниях
Жидкость

Газ

И твердое тело

Разница между ними определяется расстоянием между молекулами.
В газообразных веществах молекулы расположены далеко друг от друга

В жидкостях молекулы располагаются ближе друг к другу

В твердых телах молекулы расположены совсем близко друг к другу

Общая картинка

Переход вещества в разные состояния - это физический процесс. Само вещество не меняется, а меняется только положение молекул и/или атомов в нем.
Процесс перехода вещества из одного состояния в другое, как правило, связано с изменением температуры
нагреванием

или охлаждением

Самый простой пример, доступный в домашних условиях, - вода.
При обычной комнатной температуре водя является жидкостью

Если поместить емкость с водой в морозилку, она превратиться в лед. Лед - это вода в твердом состоянии

А если поставить чайник или кастрюльку с водой на плиту, то можно увидеть водяной пар. Водяной пар - это газообразное состояние воды

Облака - это тоже водяной пар.

Дождь - вода в жидком состоянии

А снег - это та же вода, но в твердом состоянии

Вода достаточно просто переходит из одного состояния в другое. И наш первый опыт будет именно с водой.
Сначала мы заморозим кубики льда. Потом нагреем воду, чтобы она была горячей, но не кипела.
Перельем воду в банку

Пока вода нагревается, переложим лед в тарелку
Накроем банку с водой тарелкой со льдом

Чтобы получить облако в банке, необходимо бросить в нее зажженную спичку. Дым от спички создаст ядра конденсации, на которые будет оседать водяной пар.
Вода конденсируется не только внутри банки, но и на ее стенках. Постепенно, по мере остывания, вода на стенках банки начнет стекать.
Растворимость
Это способность веществ образовывать однородные системы с другими веществами.
При растворении вещество не меняется качественно. Вещество при этом не меняется и не переходи из одного состояния в другое.

Одни вещества хорошо растворяются в воде, другие - в спирте, третьи - в масле.
Некоторые вещества вообще не могут растворять. Например, песок

Растворимость веществ в воде зависит от самого вещества, температуры, наличия примесей в растворителе и давления.
С растворимостью можно провести пару опытов.
Опыт первый. Зависимость растворимости от температуры
Нам потребуется: Поваренная соль или сахар. Вода разной температуры.
Ход опыта.
Часть воды охладите, часть воды вскипятите.
Налейте несколько стаканов с водой. Воды в стаканах должно быть одинаковое количество.
Чайными ложками добавляйте в воду сахар или соль. Для того, чтобы они быстрее растворялись, перемешивайте растворы.
Чем холоднее вода, тем меньшее количество ложек соли или сахара в ней раствориться.
Опыт второй. Зависимость растворимости от характера вещества
Нам потребуется: соль, мел и вода.
Ход опыта.
Мел раскрошите.
Налейте в стаканы одинаковое количество воды.
Добавляйте в один стакан мел, в другой стакан соль.
Добавляйте соль, пока она не перестанет растворяться.
Нагрейте полученные растворы. Соль при нагревании будет продолжать растворяться, а мел не будет растворяться даже при нагревании.
Если мел перемешать в воде, получится взвесь. Но, если оставить стакан в покое, рано или поздно мел осядет на дне стакана.
Опыт третий. Зависимость растворимости от характера растворителя
Нам потребуется: любые зеленые листья, водка, масло, вода.
Ход опыта.
Налейте в 3 стакана одинаковое количество воды, масла и водки.
Положите в жидкости одинаковое количество листьев.
Оставьте на некоторое время.
Посмотрите, что произошло.
Стакан с водкой наиболее интенсивно окраситься в зеленый цвет, т.к. хлорофилл из листьев лучше растворяется в спирте.
***
Растворенное в жикости вещество влияет на свойства самого растворителя.

Например, вода с солью кипит при большей, а замерзает при более низкой температуре.
По этому поводу мы проведем еще пару опытов.
Опыт первый. Кипение
Нам потребуется: вода, кастрюлька, соль, газовая плита.
Ход опыта.
Налейте в кастрюльку воду и поставьте ее на газ.
Дождитесь, когда вода практически закипит, но еще не бурлит.
Насыпьте в воду столовую ложку соли. Сначала вода вскипит, а затем, чтобы дойти до точки кипения нагревать воду надо будет дольше.
Похожий опыт можно провести, если одновременно поставить на газ пару кастрюлей: одну с чистой водой, вторую с раствором соли. Кастрюльку с раствором соли нагревать до кипения нужно дольше.
Опыт второй. Таяние льда
Нам потребуется: лед, сухой пищевой краситель, соль с крупными кристаллами.
Ход опыта.
Сначала заморозим лед. Замораживайте лед не маленькими кубиками, а большим куском. Мы замораживали в 200-граммовых баночках из-под сметаны и йогурта.

Если пищевой краситель в таблетках, разотрите его в порошок. Если кристаллами, то просто смешайте его с парой чайных ложек соли.
Вытащите замерзший лед из формы. Сверху насыпьте цветную соль

И ждите.
В том месте, где лед и соль соприкасаются, лед будет таять быстрее.
А в следующий раз я расскажу про чисто химические опыты в домашних условиях.